FDA 注册要求变得容易。
美国食品药品监督管理局(FDA)负责通过监管进口产品来保护公众健康。任何计划在美国市场分销食品和饮料(包括膳食补充剂和动物食品)药物、医疗和精选其他产品的公司都必须向 FDA 注册。

如果您生产以下类别的产品,FDA 注册可能是强制性的:
- 餐饮(包括膳食补充剂和动物食品)
- 医疗器械
- 药品(包括非处方药)
- 烟草产品
- 辐射类电子设备 (RED)
- 生物制品
每个产品类别都有特定的豁免,Registrar Corp可以帮助您确定是否必须注册您的设施。一些设施,如食品和饮料生产商,必须在将产品运送到美国之前向FDA注册,并在10月1日至12月31日之间每偶数年更新一次FDA注册。

通过向FDA注册您的设施,有助于促进消费者安全,并确保您的公司符合FDA要求。FDA注册涉及提交有关产品、生产设施和流程、质量控制、标签、召回程序等的详细信息。
FDA合规似乎既耗时又复杂,但不一定如此。超过30,000家食品和饮料、膳食补充剂、药物、医疗器械和化妆品公司信任Registrar Corp帮助他们轻松遵守FDA注册法规。
作为食品和饮料行业的一部分,膳食补充剂受FDA监管。这意味着,如果您是一家膳食补充剂制造商、加工商、包装商或仓库设施,试图进入美国市场,您需要向 FDA 注册您的设施。
与食品和饮料设施一样,膳食补充剂生产商、加工商、包装商和仓库设施必须在将产品运送到美国之前向FDA注册,并在每偶数年的10月1日至12月31日期间更新一次FDA注册。

Registrar Corp的膳食补充剂注册服务
我们为膳食补充剂公司提供的 FDA 设施注册服务包括:
- FDA注册和更新协助
- DUNS号码协助
- 24/7美国代理服务
- 预先申报提交

药品设施注册
在FDA注册您的药物生产设施帮助您将安全合规的产品推向市场。对于在美国生产、制备、传播或复合药品以供商业分销的所有国内外公司,必须进行 FDA 注册。
药品机构必须在药品运送到美国之前向FDA注册,并且必须在每年10月1日至12月31日期间更新注册。此外,企业必须在更新注册时提交在美国商业销售的每种药物的清单。
药物主文件提交
主文件是将专有产品数据安全、保密地提交给监管机构,例如美国食品药品监督管理局 (FDA)、加拿大卫生部或中国国家药品协会 (NMPA)。
药物主文件(DMF)包括以下信息:
- 原料药和产品
- 包装材料
- 辅料和制备材料
- 设施及其程序
- 及更多
Registrar Corp提供电子通用技术文件(eCTD)格式的DMF准备,并提交给全球18个监管机构。
生物制剂机构注册
FDA 要求人类细胞、组织和细胞/组织产品 (HCT/P) 以及血液机构制造商在生物制剂评估和研究中心 (CBER) 注册。这些注册与药物建立要求分开,涉及提交和记录的独特标准。
Registrar Corp 协助生物制剂机构履行 FDA 注册和持续合规义务。通过管理所需的备案和更新,我们帮助组织保持对 CBER 期望的合规性,同时避免对运营和市场准入造成代价高昂的干扰。

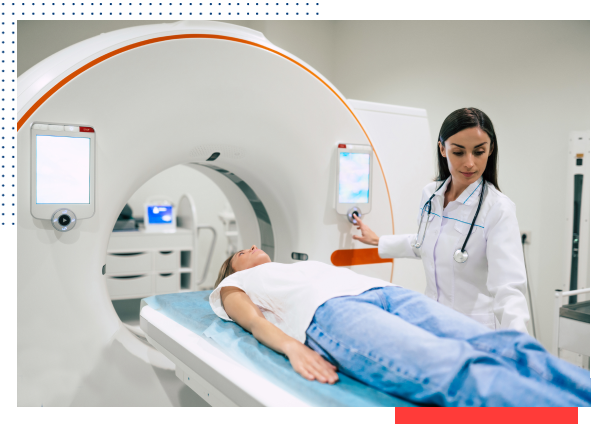
医疗器械注册
了解有哪些医疗设备可以影响美国应对公共卫生突发事件的能力。所有涉及生产和分销拟在美国使用的医疗器械的机构都需要向 FDA 注册。
医疗器械公司必须在将产品运送到美国之前向FDA注册,并且必须在每年10月1日至12月31日期间更新注册。

医疗器械主文件提交
与药物主文件类似,医疗器械主文件 (MAF) 包含专有产品数据,可安全地提交给国家和国际监管机构。
MAF包括以下方面的信息:
- 设施及其程序
- 器械配方
- 包装材料
- 临床和非临床研究数据
- 及更多
Registrar Corp提供电子通用技术文件(eCTD)格式的MAF准备,并提交给全球18个监管机构。
Registrar Corp的医疗器械注册服务
通过我们的 FDA 医疗设备设施注册服务,您可以获得:
- FDA注册和更新协助
- UDI和GUDID协助与合规
- 24/7美国代理服务
- 电子医疗设备报告(eMDR)

注册证书
公司注册后,FDA将签发注册号,但不提供注册证书。然而,许多买家或进口商仍然要求供应商进行注册确认。
如果您的机构已经向FDA注册,Registor Corp可以提供第三方注册证书,以向买家、报关行和供应商确认您的FDA注册有效。我们目前为食品和饮料、药品和化妆品行业的公司提供第三方注册证书。
如果您的企业还未在FDA注册,请考虑与Registrar Corp合作注册您的企业,并获得第三方注册证书。
验证您的FDA注册
FDA注册号可能会意外失效,并导致在入境口岸的延误或扣留。您的 FDA 注册号可能无效的原因包括:
- 过时的所有权或其他信息
- 未由授权人员提交注册
- 企业的美国代理人拒绝指定
- 未在续约截止日期前更新注册
Registrar Corp免费提供美国FDA注册验证。您可以方便快捷地检查贵企业的注册是否有效,并采取纠正措施以防止潜在的费用或罚款。


合规确认
当产品到达美国入境口岸时,必须以电子方式提供特定信息并传送给美国海关和边境保护局(CBP)。如果产品受 FDA 监管或可能受 FDA 监管,CBP 会将进口入境信息发送给 FDA 进行验证。
适当的合规确认(AofC)代码和限定符可以加快受理流程。虽然这些AofC代码的使用是自愿的,但它将有助于加快入境审查流程,并增加根据进口系统筛查处理货物的可能性。